L'imagerie médicale nouvelle génération
Une cartographie du fer cérébral robuste et performante
Exploration de marqueurs neurologiques
Le fer, au cœur des
maladies cérébrales
Le fer cérébral joue un rôle clé dans de nombreuses pathologies neurologiques, mais sa quantification reste complexe et débattue.
Les techniques d’imagerie conventionnelles fournissent peu de précision sur sa distribution fine.
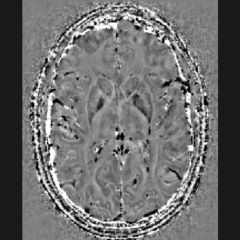
Nos solutions permettent de cartographier le fer in vivo, offrant des mesures fiables et reproductibles pour explorer son implication dans la neurodégénérescence.
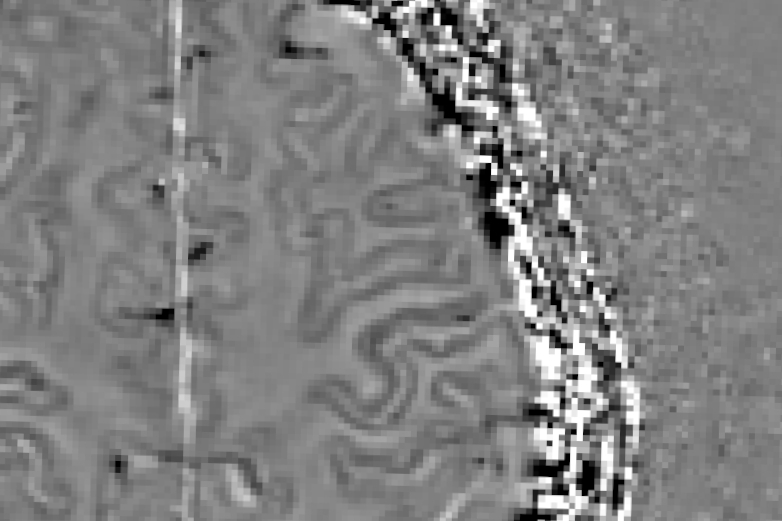
SUIVI DU FER DANS LES MALADIES CÉRÉBRALES
La maladie d’Alzheimer est une maladie neurodégénérative évolutive affectant diverses régions cérébrales.
Le processus physiopathologique implique une accumulation de peptides Aβ et de protéines Tau associés à une modulation du fer intracérébral.
Aux côtés des biomarqueurs protéiques Aβ, Tau et phospoTau, l’imagerie médicale par PET-Scan permet une visualisation des agrégats de peptides Aβ et de protéines Tau. Les accumulations de fer peuvent être visualisées et quantifiées sans injection de produit de contraste en utilisant la technologie d’IRM BIaaS (Brain-Iron-as-a-Service).
Cette quantification du fer par BIaaS dans les régions intracérébrales profondes est potentiellement liée à des stades précoces prodromaux de la maladie. Notre solution BIaaS pourrait permettre une détection plus précoce et améliorer le suivi longitudinal des patients. Cette technologie présente aussi un intérêt fort pour le suivi thérapeutique et le suivi des effets secondaires des thérapies innovantes.
La maladie de Parkinson est une maladie neurodégénérative due à la formation d’agrégats de protéine α-synucléine dans les neurones.
Associé à cette agrégation, il a été aussi montré une accumulation de fer intracérébral.
Le diagnostic de cette maladie repose généralement sur des signes tels que des tremblements au repos, une rigidité des membres, une akinésie et des troubles de la marche.
L’imagerie cérébrale, généralement par IRM, se limite souvent à exclure la présence d’une autre étiologie. Une scintigraphie cérébrale peut permettre de mettre en évidence la perte de neurones dopaminergiques.
La quantification des accumulations de fer intracérébral par IRM dans la substance noire/substantia nigra est bien documentée.
La démence vasculaire est une maladie neurodégénérative dont l’étiologie est multiple. Les lésions du tissu nerveux cérébral peuvent être dues à des lésions ischémiques impliquant des petits vaisseaux, à des infarctus multiples, à un déclin cognitif après un accident vasculaire cérébral ou à l’association de ces déficits et d’une autre maladie neurodégénérative de type Alzheimer.
Comme de nombreuses démences, le diagnostic est basé sur l’évaluation clinique du sujet, sur une dégradation des fonctions cognitives par palier et une évaluation par imagerie médicale.
BIaaS (Brain-Iron-as-a-Service), par sa capacité à mettre en évidence les microsaignements peut apporter une information objective sur l’étiologie de la maladie.
La sclérose en plaques est une maladie auto-immune liée à la présence de lésions de la substance blanche associée à une inflammation chronique induisant une démyélinisation.
Il a été montré dans les lésions actives et inflammatoires, une accumulation de fer.
Le diagnostic est basé sur l’utilisation de l’IRM pour visualiser et qualifier les lésions. Néanmoins la corrélation entre le nombre de lésions, leur types et la gravité des symptômes reste complexe à établir.
BIaaS (Brain-Iron-as-a-Service) permet de visualiser les accumulations de fer dans les lésions et de catégoriser celles-ci en termes d’activité et d’évolution. Cette solution pourrait aussi participer à la caractérisation du signe de la veine centrale (SVC).
La manifestation du fer, à travers le signe de la veine centrale et le halo paramagnétique, fait désormais partie des critères internationaux de McDonald pour diagnostiquer et suivre la SEP (version révisée en septembre 2025).
Les neurodégénérescences par accumulation intracérébrale de fer (NBIA) forment un ensemble de maladies génétiques caractérisées par une accumulation constante de fer dans des régions spécifiques du cerveau. Les neuroferritinopathies et les acéruloplasminémies sont les deux principales catégories de mutations mais il existe de nombreuses voies métaboliques impliquées dans cette famille de maladies : métabolisme des lipides, fonctionnement des mitochondries, activité lysosomale et autophagie.
Le diagnostic est complexe, la diversité des symptômes est importante et les processus physiopathologiques sont multiples.
L’accumulation de fer en intracérébral est le point commun de cette famille de pathologies. La quantification de cette accumulation par IRM pourrait être utilisée comme une méthode diagnostic et de suivi de nouvelles thérapies.
La maladie de Huntington est une maladie neurodégénérative rare et héréditaire. Il existe une forme adulte et une forme juvénile encore plus rare. Elle se caractérise par des troubles moteurs et cognitifs.
Le diagnostic de la maladie de Huntington est basé sur le contexte familial et des signes évocateurs. L’imagerie par PET-Scan et par IRM permet d’établir un diagnostic différentiel et d’évaluer en particulier l’atrophie du caudate et du putamen.
Une augmentation significative de fer a été montrée chez les malades dans le caudate, le putamen et le globus pallidus. BIaaS pourrait permettre le suivi de la maladies et de nouvelles thérapies.
Les traumatismes crâniens regroupent des atteintes neurologiques variées pouvant résulter d’un choc direct, de forces d’accélération‑décélération, d’hémorragies intracrâniennes ou de lésions axonales diffuses. Ces altérations peuvent entraîner un déclin cognitif, des troubles fonctionnels et, dans certains cas, des évolutions neurodégénératives tardives.
Le diagnostic repose sur l’évaluation clinique, l’évolution des fonctions cognitives et l’imagerie, en particulier la tomodensitométrie ou l’IRM. Les symptômes peuvent progresser par paliers selon l’apparition de lésions secondaires, comme les microsaignements.
BIaaS (Brain‑Iron‑As‑A‑Service), grâce à sa capacité à détecter les veines, hémorragies et les microsaignements, pourrait fournir une information objective plus précise sur la nature et l’étendue des lésions post‑traumatiques.
Une solution 100% intégrée
et compatible
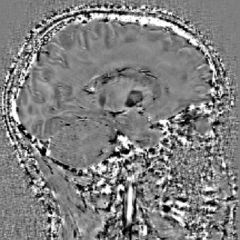
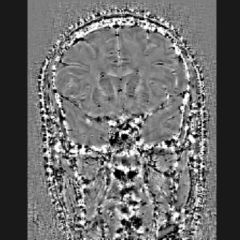
Compatible 100% IRM
Accès en mode SaaS sur Cloud sécurisé
Compatible PACS - DICOM
Marquage en tant que dispositif médical en cours
INDICATIONS ET USAGES
Étude pré-cliniques
Étude cliniques
Dispositif médical
Marquage en tant que dispositif médical en cours
Ils nous font confiance